公司相關
2026.02.07
順藥入選國際中風年會閉幕專題 創台灣首例
順天醫藥(櫃檯買賣中心代號6535)宣布,旗下腦中風新藥 LT3001 臨床二期試驗結果,獲選為國際中風年會(International Stroke Conference, ISC)最新突破性研究(Late-Breaking Science , LBS),並於閉幕大會上進行專題發表,創下台灣首例。現場將有上千專家聆聽,並由美國權威血管神經專家Dr. Thomas Devlin主講。
國際中風年會由美國心臟協會/美國中風協會主辦,長期扮演全球中風領域最具影響力的學術與臨床交流平台,匯聚國際臨床意見領袖、醫療機構與產業專家,也是重大突破性數據的關鍵發表舞台。特別是閉幕專題,向來為年會最受關注的場域,上千篇世界頂級論文僅有6篇能入選發表,順藥LT3001有幸成為其中一篇。
順藥總經理葉聖文認為,這次能在全球矚目場合發表試驗結果,有三項實質助益,首先是可望加速三期收案動能。ISC主舞台直接觸及大量具收案能力的中風中心與臨床醫師,強化臨床醫師對試驗設計與數據的理解,提升參與意願,進而擴大試驗網絡與病人轉介效率,有助縮短啟動與收案所需時間。
其次,強化全球臨床醫師對 LT3001 的認知與共識形成,因為閉幕專題有助關鍵數據在最短時間內被全球臨床社群廣泛檢視與討論,提升臨床端對順藥的作用價值、適用情境,促進後續臨床採納與研究合作。更重要的是,有全球指標性的年會與權威研究者背書,將可推進與大藥廠的合作進程,有利在授權與合作上展開更深入、加速的對話。
順藥日前針對 LT3001 中風新藥,向美國FDA進行Type C諮詢,美國FDA回函認為,主要療效指標方面,FDA表示以給藥後 90 天之 mRS 0-2 或 mRS 0-1 作為三期試驗主要療效指標均屬可接受,並完全符合國際監管實務,可作為後續藥證審查的重要依據。針對受試者人種比例,FDA並未要求特定比例之美國受試者,僅強調最終結果需具備合理外推至美國臨床族群的能力。
關於順天醫藥生技股份有限公司(6535.TWO)
順天醫藥生技股份有限公司(Lumosa Therapeutics Co., Ltd.,簡稱順藥)是一家臨床階段製藥公司,致力於開發針對具急迫未滿足醫療需求之神經系統疾病的創新治療方案與解決方案。除運用自有技術平台外,順藥亦積極投入科學授權(licensing)與共同開發合作(co-development collaboration),建立由早期至後期資產所構成的研發產品組合,涵蓋具「同類首創」(first-in-class)與「同類最佳」(best-in-class)潛力之藥物。順藥專案涵蓋已上市產品與臨床研發中資產;包括長效型術後止痛注射劑納疼解®(LT1001),目前已在台灣、新加坡、馬來西亞、泰國、烏克蘭及汶萊等多國取得核准並上市銷售;LT3001為治療急性缺血性腦中風之創新小分子藥物,是公司主要臨床開發中產品,已於美國、歐洲、中國及台灣完成多項第二期臨床試驗,展現具備延長至24小時之治療時間窗以及良好的安全性與療效表現;以及針對神經系統疾病開發之外泌體(exosome)LT6001。

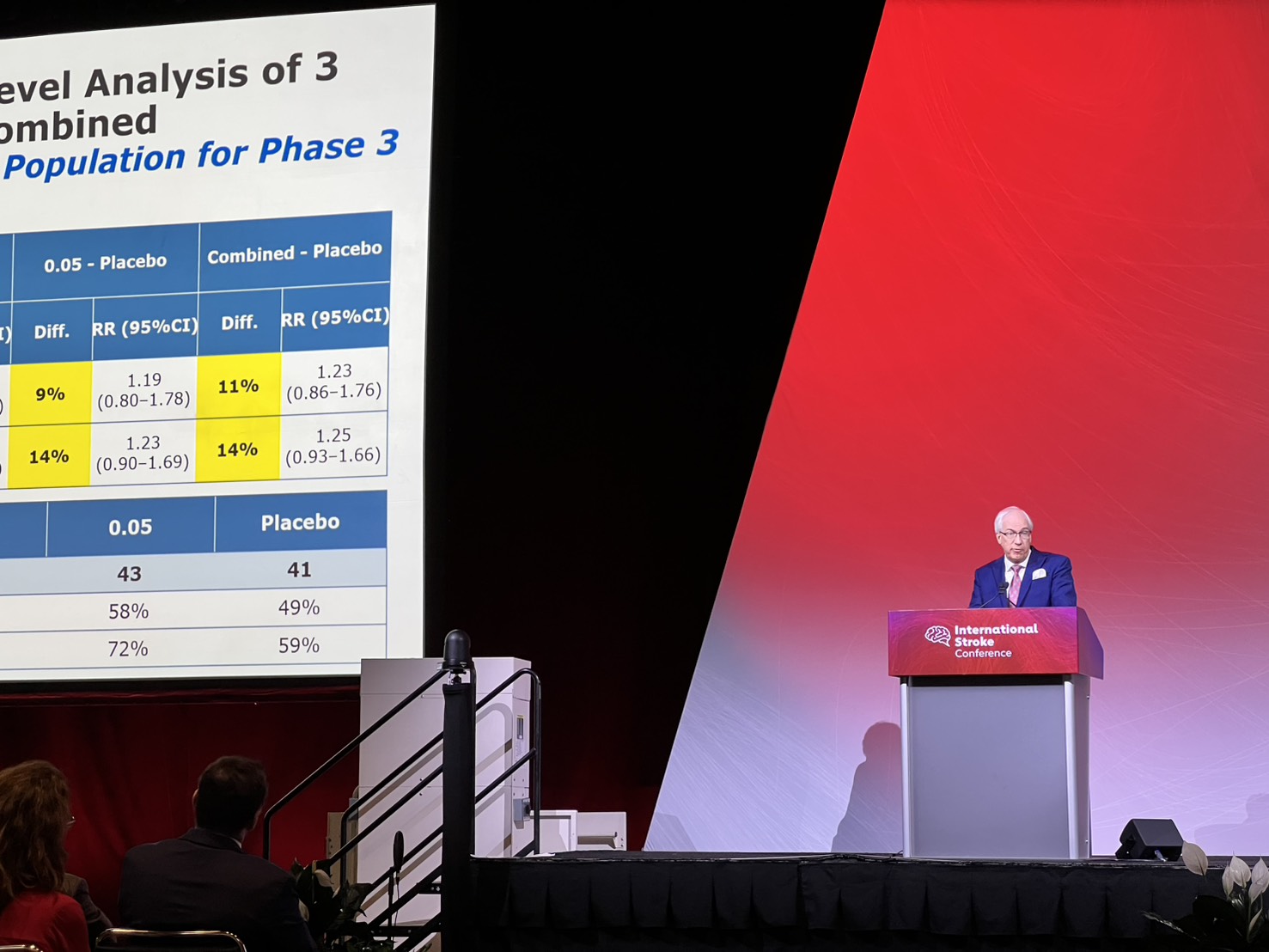

國際中風年會由美國心臟協會/美國中風協會主辦,長期扮演全球中風領域最具影響力的學術與臨床交流平台,匯聚國際臨床意見領袖、醫療機構與產業專家,也是重大突破性數據的關鍵發表舞台。特別是閉幕專題,向來為年會最受關注的場域,上千篇世界頂級論文僅有6篇能入選發表,順藥LT3001有幸成為其中一篇。
順藥總經理葉聖文認為,這次能在全球矚目場合發表試驗結果,有三項實質助益,首先是可望加速三期收案動能。ISC主舞台直接觸及大量具收案能力的中風中心與臨床醫師,強化臨床醫師對試驗設計與數據的理解,提升參與意願,進而擴大試驗網絡與病人轉介效率,有助縮短啟動與收案所需時間。
其次,強化全球臨床醫師對 LT3001 的認知與共識形成,因為閉幕專題有助關鍵數據在最短時間內被全球臨床社群廣泛檢視與討論,提升臨床端對順藥的作用價值、適用情境,促進後續臨床採納與研究合作。更重要的是,有全球指標性的年會與權威研究者背書,將可推進與大藥廠的合作進程,有利在授權與合作上展開更深入、加速的對話。
順藥日前針對 LT3001 中風新藥,向美國FDA進行Type C諮詢,美國FDA回函認為,主要療效指標方面,FDA表示以給藥後 90 天之 mRS 0-2 或 mRS 0-1 作為三期試驗主要療效指標均屬可接受,並完全符合國際監管實務,可作為後續藥證審查的重要依據。針對受試者人種比例,FDA並未要求特定比例之美國受試者,僅強調最終結果需具備合理外推至美國臨床族群的能力。
關於順天醫藥生技股份有限公司(6535.TWO)
順天醫藥生技股份有限公司(Lumosa Therapeutics Co., Ltd.,簡稱順藥)是一家臨床階段製藥公司,致力於開發針對具急迫未滿足醫療需求之神經系統疾病的創新治療方案與解決方案。除運用自有技術平台外,順藥亦積極投入科學授權(licensing)與共同開發合作(co-development collaboration),建立由早期至後期資產所構成的研發產品組合,涵蓋具「同類首創」(first-in-class)與「同類最佳」(best-in-class)潛力之藥物。順藥專案涵蓋已上市產品與臨床研發中資產;包括長效型術後止痛注射劑納疼解®(LT1001),目前已在台灣、新加坡、馬來西亞、泰國、烏克蘭及汶萊等多國取得核准並上市銷售;LT3001為治療急性缺血性腦中風之創新小分子藥物,是公司主要臨床開發中產品,已於美國、歐洲、中國及台灣完成多項第二期臨床試驗,展現具備延長至24小時之治療時間窗以及良好的安全性與療效表現;以及針對神經系統疾病開發之外泌體(exosome)LT6001。









